
慢性疼痛并不必然通向抑郁,真正决定结局的不是疼痛本身,而是大脑是否还能稳住情绪。
复旦大学类脑智能科学与技术研究院认知神经科学中心执行主任肖晓、特聘教授Trevor Robbins及冯建峰教授团队研究发现,海马齿状回像一道“情绪闸门”,疼痛早期,它短暂增强试图适应。当调控失衡,疼痛才被转化为持续的负性情绪,齿状回中新生神经元异常激活小胶质细胞参与重塑,兴奋—抑制平衡被打破,抑郁由此出现。
相关成果以《从慢性疼痛到抑郁:海马齿状回中新生神经元驱动的小胶质细胞重塑》为题,北京时间今天(3月20日)发表于《科学》(Science)主刊。
慢性疼痛不仅是一种长期存在的身体不适,更是一项重大的公共健康和社会问题。世界卫生组织和多项流行病学研究显示,全球约20%—30%的成年人正在遭受不同形式的慢性疼痛。更值得关注的是,慢性疼痛往往并非“只有疼痛本身”。大量临床调查显示,在长期疼痛人群中,约一半以上会伴随不同程度的抑郁或焦虑症状,其背后的生物学机制一直不清楚。正是在这一背景下,理解慢性疼痛如何影响大脑情绪调控系统、以及为何这种影响在不同个体之间存在巨大差异,成为神经科学、医学和公共健康领域共同关注的核心问题。
复旦团队的此项研究,通过系统整合大规模人群神经影像数据与啮齿动物慢性神经病理性疼痛模型,从脑结构、功能、神经环路及细胞机制多个层级,对慢性疼痛向情绪障碍演变的过程进行了纵向解析。
研究整合了大规模人群神经影像数据(UK Biobank)、啮齿动物慢性神经病理性疼痛模型,从脑结构、功能、神经环路与细胞机制多个层级,系统分析慢性疼痛向抑郁、焦虑发展的过程。
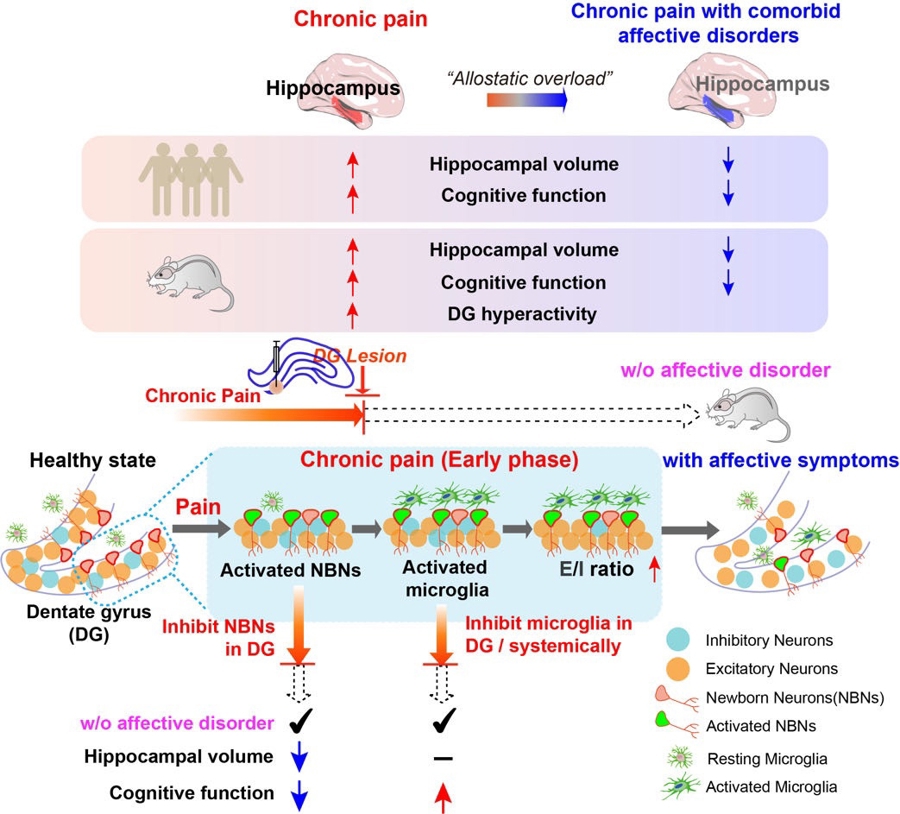 慢性疼痛向情绪共病进展的因果过程示意图
慢性疼痛向情绪共病进展的因果过程示意图
研究发现,大脑中存在一个决定性“情绪闸门”。慢性疼痛并不会直接导致抑郁或焦虑。是否发展为情绪障碍,取决于大脑情绪调控系统能否维持稳定。闸门正常,疼痛可被整合和缓冲;闸门失效,疼痛更容易转化为持续的负性情绪。
海马则是这一“情绪闸门”的核心枢纽。人群影像数据显示:疼痛早期,海马体积短暂增大,功能状态增强。疼痛持续并伴随抑郁后,海马逐渐萎缩,调控能力下降。海马中的齿状回(dentate gyrus, DG)是“情绪闸门”的关键节点。DG是成年大脑中少数仍能产生新神经元的区域,负责信息区分与整合。疼痛早期,DG内新生神经元及相关信号被激活,表现出适应性可塑性;疼痛维持期,小胶质细胞参与调控,神经环路兴奋—抑制平衡被打破,情绪调控逐渐失败。
研究比较了不同干预节点的效果:直接抑制新生神经元,可缓解情绪异常,但可能影响部分脑功能平衡。调控小胶质细胞异常激活,可缓解疼痛相关情绪问题,同时更好地维持整体功能稳定性。该研究结果提示,小胶质细胞可能是阻断慢性疼痛向情绪障碍转变的更优靶点。
研究发现,大脑中存在一个决定性“情绪闸门”。慢性疼痛并不会直接导致抑郁或焦虑。是否发展为情绪障碍,取决于大脑情绪调控系统能否维持稳定。闸门正常,疼痛可被整合和缓冲;闸门失效,疼痛更容易转化为持续的负性情绪。
海马则是这一“情绪闸门”的核心枢纽。人群影像数据显示:疼痛早期,海马体积短暂增大,功能状态增强。疼痛持续并伴随抑郁后,海马逐渐萎缩,调控能力下降。海马中的齿状回(dentate gyrus, DG)是“情绪闸门”的关键节点。DG是成年大脑中少数仍能产生新神经元的区域,负责信息区分与整合。疼痛早期,DG内新生神经元及相关信号被激活,表现出适应性可塑性;疼痛维持期,小胶质细胞参与调控,神经环路兴奋—抑制平衡被打破,情绪调控逐渐失败。
研究比较了不同干预节点的效果:直接抑制新生神经元,可缓解情绪异常,但可能影响部分脑功能平衡。调控小胶质细胞异常激活,可缓解疼痛相关情绪问题,同时更好地维持整体功能稳定性。该研究结果提示,小胶质细胞可能是阻断慢性疼痛向情绪障碍转变的更优靶点。
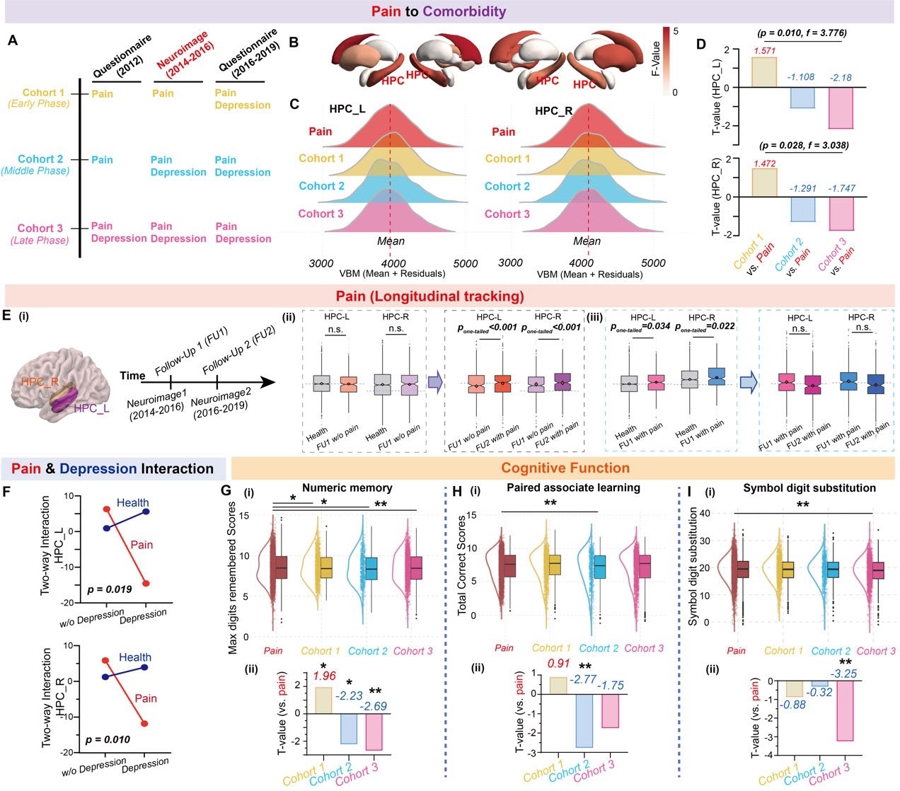 慢性疼痛向抑郁共病进展过程中海马体积变化
慢性疼痛向抑郁共病进展过程中海马体积变化
该研究得到国家科技部2030脑科学与类脑研究重大项目、国家科技部重大专项、国家自然科学基金委面上项目等项目支持。
复旦大学认知神经科学中心是张江复旦国际创新中心核心设备平台,纳入“双一流”学科重点建设,也是上海市级科技重大专项“脑与类脑智能基础转化应用研究”的重要依托平台。该中心是国内首个同时具备脑认知机制解析与计算仿真能力的交叉研究平台,致力于成为国际脑科学合作的重要节点。
千里马配资提示:文章来自网络,不代表本站观点。